 |
|
|
|
シクロデキストリン(CD)を用いた超分子合成 |
| 修飾CDを用いた超分子錯体の合成 | CDによる高分子鎖の認識挙動の解明 | ||
| 外部刺激による超分子錯体の構造制御 | 超分子エネルギー変換システムの開発 | ||
| 共役分子を有す超分子錯体の合成 | Social Self-Sorting型超分子錯体CD | ||
| シクロデキストリンを用いた並進・回転運動の観察 | 挿し違いダイマー |
Social Self-Sorting 型超分子錯体
これまでに我々は、ホスト分子であるシクロデキストリン(CD)に二級水酸基の3
位にアミド結合にてゲスト分子を導入した一置換修飾CDの水中における超分子ポリ
マー形成について報告してきた。我々はCDの二級水酸基の置換位置により、形成され
る超分子錯体の構造が異なるのではないかと考え、桂皮酸をα-CDの二級水酸基の2位
または3位にエステル結合にて導入し、超分子錯体形成挙動について調査
した。
その結果、2位または3位に修飾された桂皮酸エステルが転位反応を示すだけ
でなく、単独状態と混合状態により形成される超分子錯体が異なるといった興味深い
挙動を示した。
![広い口側の二級水酸基にゲスト分子が修飾されたCDによるポリ[2]ロタキサン合成](images/Social_self_sorting.gif)
Tomimasu, N.; Kanaya, A.; Takashima,Y.; Yamaguchi, H.; Harada, A.
"Social Self-Sorting: Alternating Supramolecular Oligomer Consisting of Isomers"
J. Am. Chem. Soc. 2009, 131(34), 12339-12343.
8mM以上の単独状態において、2-CiO-α-CDは挿し違い型の二量体を形成していることがX線構造解析から明らかとなり、3-CiO-α-CDは2D ROESY NMR、PFG NMRの測定の結果、桂皮酸部位が二級水酸基側から包接された超分子ポリマーを形成していることが示唆された。
2-CiO-α-CDと3-CiO-α-CDを等量ずつ混合した水溶液においては2-CiO-α-CDの桂皮酸部位と3-CiO-α-CDのCD部位、2-CiO-α-CDの桂皮酸部位と3-CiO-α-CDのCD部位とお互いが交互に包接された構造であることが2D ROESY NMRから示唆された。
また、形成された超分子錯体の分子サイズを求めるためにPFG NMRを測定した結果からヘテロ超分子ポリマーを形成が示唆された。
このようにCDは2位と3位に修飾された置換基を厳密に見極め、新たな超分子錯体を形成することが明らかとなった。
光刺激に応じた超分子ポリマーの配列制御
単糖におけるアシル基転位反応は広く知られているが、α-D-グルコースを構成ユニットにもつ環状オリゴ糖であるシクロデキストリン(CD)のアシル基転位反応についての詳細な報告はない。本研究ではアシル基としてαCD と会合定数の高いスチルベンをその二級水酸基に導入したところ、アシル基の転位反応によって生じる化合物のそれぞれが異なる超分子錯体を形成していることが明らかとなった。さらに今回、スチルベンの異性体に応じて転位速度が異なり、この速度が超分子構造に影響を受けていることを観察した。
2-StiO-αCD と3-StiO-αCD は置換基であるアシル基(スチルベンカルボニル基)の転位反応により、重水中及び重DMSO 中で互いに異性化することが1H NMR により確認された。重水中45 ℃の平衡状態における2-StiO-αCD と3-StiO-αCD の存在比は17:3 であった([2-StiO-αCD] + [3-StiO-αCD] = 1 mM)。また、重水中における転位速度は溶液濃度に依存し、高濃度におけるほど抑制されることが確認された。更に、紫外光照射 (λ = 320 nm)によりスチルベン部位をトランスからシスに光異性化させスチルベン部位とCD 部位との会合力を低下させると、トランス体よりも転位速度が加速されることが分かった。
以上から、超分子錯体形成によってアシル基の転位反応が抑制されることが示された。そこで、形成される超分子錯体の構造を調べるために2D ROESY NMR 測定を行ったところ、2-StiO-αCD と3-StiO-αCDの混合溶液中においても同じ異性体同士(2-StiO-αCD 同士、及び3-StiO-αCD 同士)でホモ超分子錯体形成をすることが明らかとなった(図1).
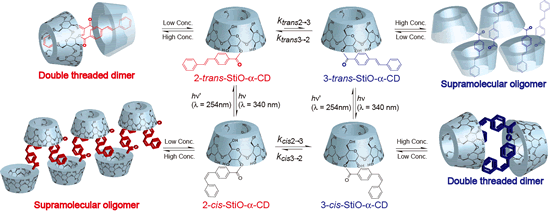
Kanaya, A.; Takashima, Y.; Harada A.
"Double Threaded Dimer and Supramolecular Oligomer Formed by Stilbene Modified Cyclodextrin – Effect of Acyl Migration and Photo Stimuli"
J. Org. Chem., 2011, 76, 492-499.