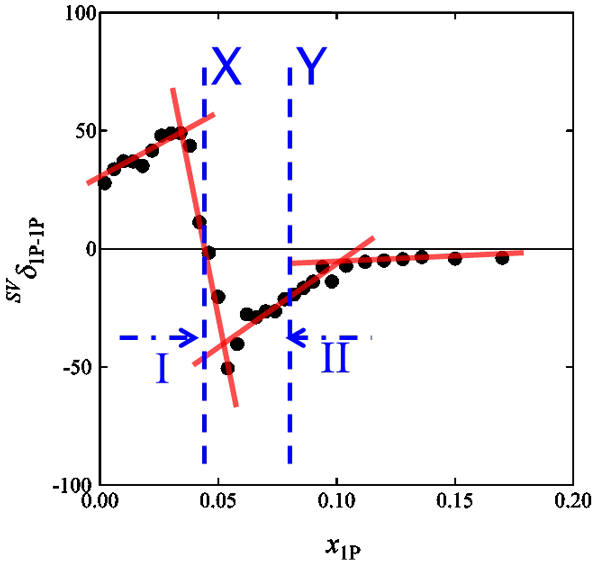
 Fig. 1. SVδ1P-1P for aqueous 1-propanol.
Fig. 1. SVδ1P-1P for aqueous 1-propanol.
ギブズエネルギー G は系全体の熱力学的な情報をすべて含んでおり,(T,p,nB)を独立変数とする系でも,多体問題の理解に対して威力を発揮します.それには G を適切な独立変数で偏微分することで,実験精度の許す限り高次の微分量を観測することにより,系のさらに詳細な情報を取り出すことができます.水や水溶液に関する G の高次微分量を得ることにより,溶質の個性だけでなく,水の水素結合ネットワークの挙動をより詳しく調べることを期待しています.
 Fig. 1. SVδ1P-1P for aqueous 1-propanol.
Fig. 1. SVδ1P-1P for aqueous 1-propanol.
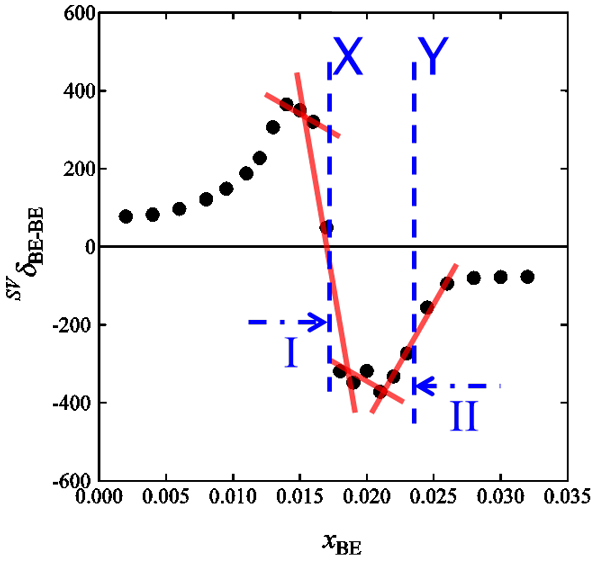 Fig. 2. SVδBE-BE for aqueous 2-butoxyethanol.
Fig. 2. SVδBE-BE for aqueous 2-butoxyethanol.
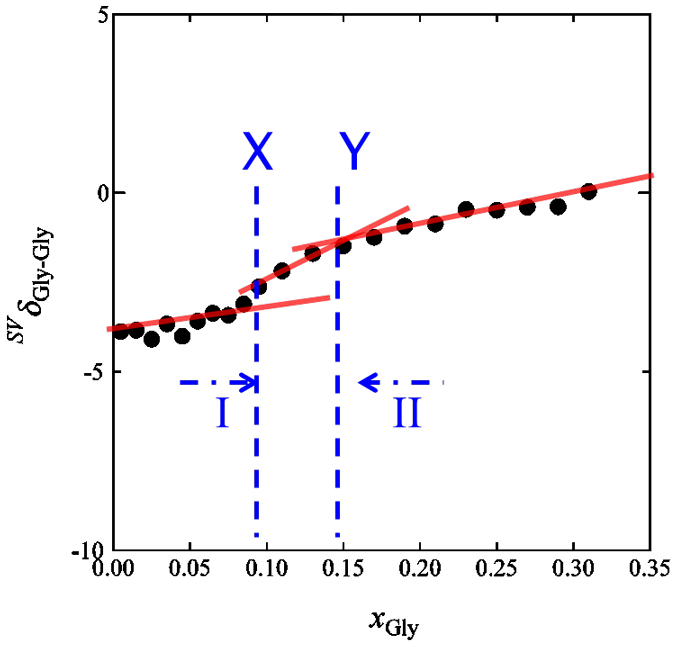 Fig. 3. SVδGly-Gly for aqueous glycerol.
Fig. 3. SVδGly-Gly for aqueous glycerol.
私たちはこれまで,G の3次微分量のひとつで,部分モルエントロピー・体積相互揺らぎ密度,SVδB,を幾つかのアルコール水溶液について 25 °C で直接測定を行ってきました(No. 31 (2010),研究紹介12).その結果,系全体に広がる水の水素結合ネットワークが保持している状態(Scheme I)から,水素結合ネットワークが切断された状態(Scheme II)への移行と思われるピークや折れ曲がりが SVδB に見られました.しかし,グリセロール水溶液では,それが十分に明瞭ではありませんでした.
そこで今回は,SVδBの変化をより詳しく見るため,SVδB をさらに濃度で微分した SVδB-B を求めました.SVδB-Bは G の4次微分量に相当し,以下の式によって定義されます.
1–プロパノール,2–ブトキシエタノール,グリセロール水溶液について得られた SVδB-B をそれぞれ Fig. 1,Fig. 2,Fig. 3 に示します.1–プロパノールと2–ブトキシエタノールの水溶液では,SVδBのグラフで見られたピークの位置(X)や折れ曲がり点(Y)は,より明確に見ることができました.X 点が Scheme I の終わり,Y 点が Scheme II の始まりであると考えられます.Scheme I では,濃度が上がるにつれて SVδB-Bは増加しますが,1–プロパノールと2–ブトキシエタノールとでは挙動が異なることがわかります.後者は X 点付近でもう一つ構造があるようにも見えます.
一方グリセロールの結果を見ると,SVδB では見えにくかった Scheme I の終わりが,SVδB-Bではステップの中点として見ることができます.G の4次微分である SVδB-B を求めることより,グリセロール水溶液でも Scheme I の終わりを確認することができました.
K. Yoshida, S. Baluja, A. Inaba, K.Tozaki, and Y. Koga, 6th International & 8th Japan-China Joint Symposium on Calorimetry and Thermal Analysis (CATS2011) (Hachiouji), 048 (2011).
Copyright © Research Center for Structural Thermodynamics, Graduate School of Science, Osaka University. All rights reserved.