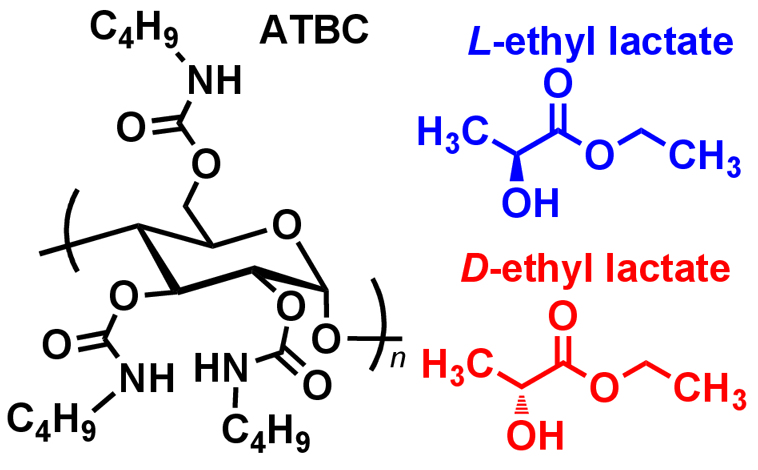
 Chart. 1. Chemical structures of 1: amylose tris(n-butylcarbamate) (ATBC), 2: L-ethyl lactate (L-EL), 3: D-ethyl lactate (D-EL).
Chart. 1. Chemical structures of 1: amylose tris(n-butylcarbamate) (ATBC), 2: L-ethyl lactate (L-EL), 3: D-ethyl lactate (D-EL).
医薬品には,光学活性物質が多く,かつ薬として効くのは片方の鏡像体のみで,他方は人体に害となる場合も数多く存在します.したがって,特に薬学分野において,キラル分離クロマトグラフィーはなくてはならない技術です.
 Chart. 1. Chemical structures of 1: amylose tris(n-butylcarbamate) (ATBC), 2: L-ethyl lactate (L-EL), 3: D-ethyl lactate (D-EL).
Chart. 1. Chemical structures of 1: amylose tris(n-butylcarbamate) (ATBC), 2: L-ethyl lactate (L-EL), 3: D-ethyl lactate (D-EL).
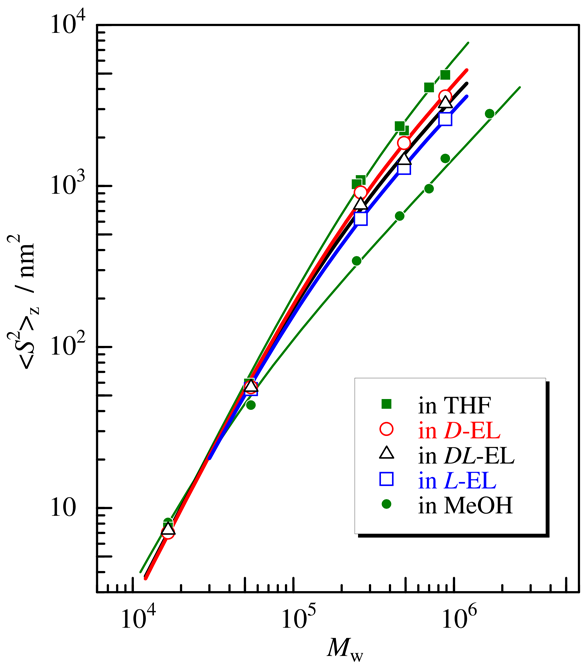 Fig. 1. Molecular weight dependence of 〈S 2〉z for ATBC in D-EL (open circles), DL-EL (triangles), L-EL (open squares), THF (filled squares), and MeOH (filled circles) at 25 °C. Curves: theoretical values calculated for the wormlike chain model.
Fig. 1. Molecular weight dependence of 〈S 2〉z for ATBC in D-EL (open circles), DL-EL (triangles), L-EL (open squares), THF (filled squares), and MeOH (filled circles) at 25 °C. Curves: theoretical values calculated for the wormlike chain model.
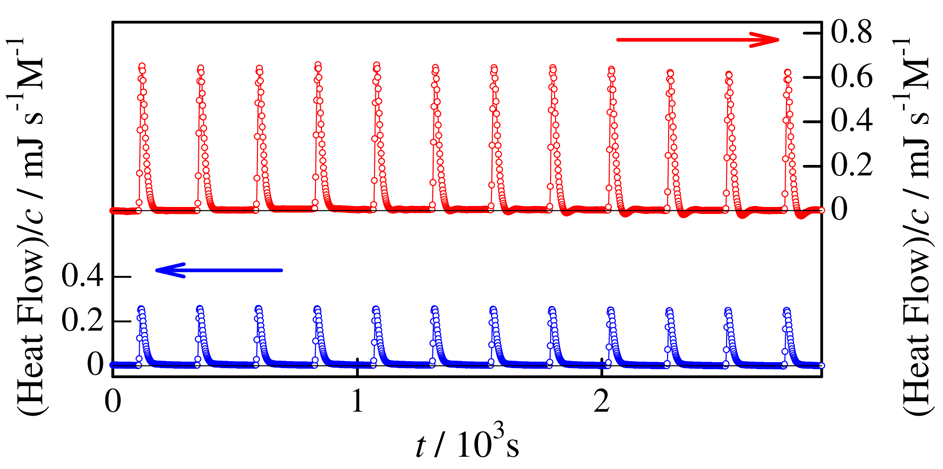 Fig. 2. Isothermal titration calorimetric data for ATBC in L-EL (top) and D-EL (bottom) at 25 °C. 2 µL solution was dropped at every 2 min.
Fig. 2. Isothermal titration calorimetric data for ATBC in L-EL (top) and D-EL (bottom) at 25 °C. 2 µL solution was dropped at every 2 min.
アミロースおよびセルロースのカルバメート誘導体やエステル誘導体は,この光学活性物質のキラル分離カラムの担体として広く利用されています.これらの多糖誘導体担体のキラルな表面が,種々の光学活性物質と多点で水素結合や双極子・双極子相互作用して,高い分離能を発現しています.そして,キラルな表面の微視的構造は,多糖の分子形態によって決まり,また一方では,多糖の分子形態自身は,光学活性物質と相互作用によって変化する可能性があります.すなわち,キラル分離カラムの分解能は,多糖誘導体と光学活性物質の相互の影響によって決まっているといえます.
本研究では,アミロース誘導体の一種であるアミローストリス(n-ブチルカルバメート)(ATBC; Chart 1 の1)の L-エチル乳酸(L-EL; Chart 1 の2)と D-エチル乳酸(D-EL; Chart 1 の3)中での分子形態と高分子−溶媒間の相互作用を詳細に調べ,溶媒の不斉構造の違いがアミロース誘導体の分子形態に及ぼす効果について調べました.
Fig. 1 には,光散乱及び小角X線散乱によって決めた ATBC の L-EL 中,D-EL中,およびそれらのラセミ混合物 DL-EL 中での二乗平均回転半径 〈S 2〉z の分子量 Mw 依存性を示しています.これらの乳酸エチル中での 〈S 2〉z は,すでに報告されている THF 中およびメタノール(MeOH)中での結果の中間の値をとっていますが,L-EL 中,DL-EL中,D-EL 中の順に少しずつ大きくなっています.鏡像体は,物理的・化学的性質にほとんど差がありませんので,この光学活性溶媒中での ATBC の広がりの違いは,高分子と溶媒のキラルな相互作用に基づいていると考えられます.
Fig. 2 には,ATBC の L-EL 溶液に D-EL を滴下して希釈した際の吸熱量(上段の曲線),および D-EL 溶液に L-EL を滴下した際の吸熱量(下段の曲線)の時間変化を示します.明らかに前者の方が吸熱量が多いことがわかります.これは,ATBC と D-EL との相互作用の方が,ATBC と L-EL 間の相互作用よりも高分子をより安定にすることを意味しています.ATBC が D-EL 中でより多くの分子内水素結合を形成していると仮定しますと,この結果をうまく説明できます.また,D-EL 中で ATBC がより多くの分子内水素結合を形成していれば,鎖の剛直性は高くなるはずであり,Fig. 1 の結果とも首尾一貫しています.
Copyright © Research Center for Structural Thermodynamics, Graduate School of Science, Osaka University. All rights reserved.