研究成果 -Reserch-
糖ペプチド誘導体の合成
当研究室では、糖ペプチド誘導体の合成についても検討しています。Fig.1に示しましたように、ペプチドシンセサイザーでペプチドを合成し、そしてシステイン残基のもつチオール基とブロモアセトアミド(あるいはヨードアセトアミド)基を糖鎖の還元末端に有する糖鎖と反応させ、ペプチドに糖鎖を結合させます。この反応は、Flitschらにより単糖(GlcNAc)を用いて開発された有用な方法で、それを当研究室が有する複合型糖鎖に応用したものです。ハイマンノース型のような大型糖鎖を、タンパク質上のシステイン残基にハロアセトアミド法で結合させた例としては、理化学研究所の伊藤、松尾グループの成果が知られています。
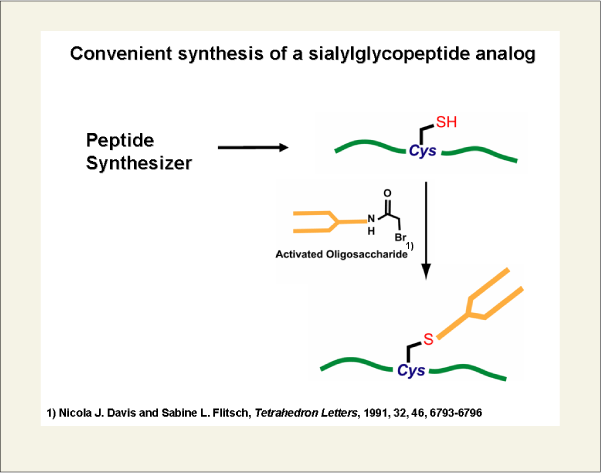
fig1
我々が行ったブロモアセトアミド基を有する複合型糖鎖の調製法をFig.2に示します。
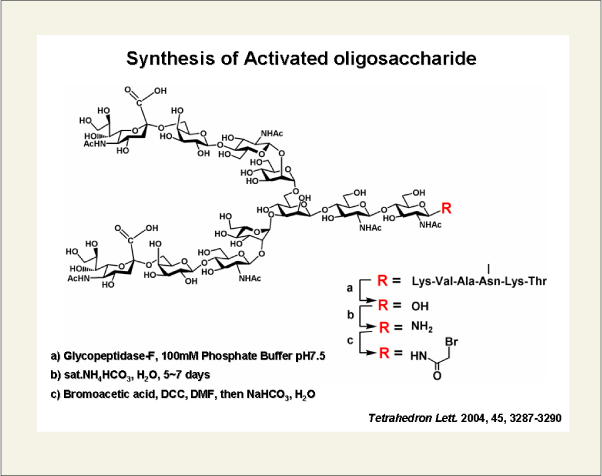
fig2
鶏卵からシアリル糖鎖ペプチドを単離後、Glycopeptidase-Fを用いて糖鎖とペプチドの間のアミド結合を加水分解し、1位が水酸基となった糖鎖を調製します。そして、炭酸水素アンモニウム等で処理し、Fig.2に示したブロモアセチル基を有する糖鎖を合成しました。
Fig.3には、シンセサイザーで合成したペプチドへの糖鎖の反応が示してあります。
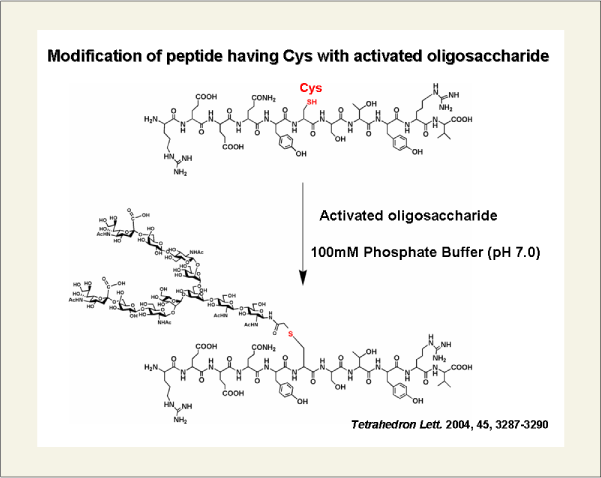
fig3
この反応は、リン酸緩衝溶液中で混ぜるだけで瞬時に完了します。また、得られた糖鎖ペプチド誘導体は、天然型の糖鎖の結合様式と比べるとアスパラギン残基の側鎖に比べ炭素1つと硫黄原子が1つ余分に含まれる誘導体です。このため、糖鎖ペプチドの代謝酵素に対して耐性を示します。Fig. 4.のグラフの各縦軸は酵素により分解されていく過程で、反応系内に残っている糖鎖ペプチドを表しています。このように、システインに糖鎖を結合させた誘導体は代謝酵素に耐性を示すので、糖鎖ペプチド製剤の開発に期待できます。
同様に、Fig.4に示したように、発現法により調製したタンパク質を本手法により糖鎖で修飾することで、糖タンパク質製剤の開発が検討できます。
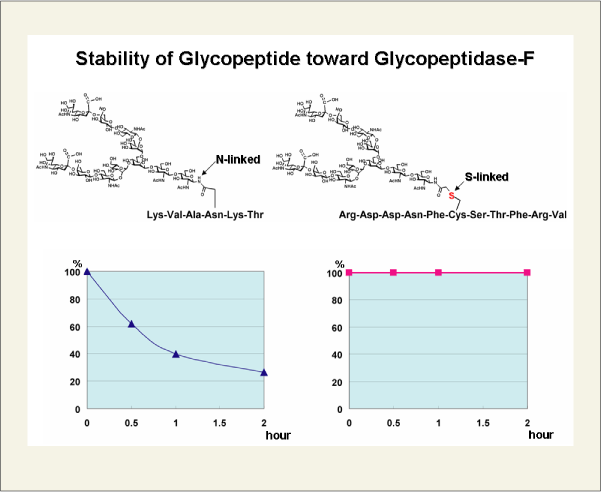
fig4
タンパク質にシアリル糖鎖を結合させると、シアル酸の酸性により血中寿命が延び、少量の投与で生理活性が期待できます。貧血治療薬であるエリスロポエチンは、複合型の4分岐シアリル糖鎖を5本持つよう改変されたもので、その結果、血中寿命が遅延され大ヒット製剤となりました。最近では、ポリエチレングリコール(PEG)を生理活性タンパク質に化学的に結合させエリスロポエチンと同様血中寿命の遅延効果を期待したものが開発されています。代表的な例はC型肝炎の治療薬として期待されているインタフェロン等がアメリカのFDAにより承認されています。今まで工業用にヒト型糖鎖を大量に利用することが困難であったために、糖鎖に変わるものとしてPEGが開発されてきましたが、ペプチド、タンパク質へヒト型糖鎖を容易に結合できるようになったので、今後の下図のような研究開発が期待されます。
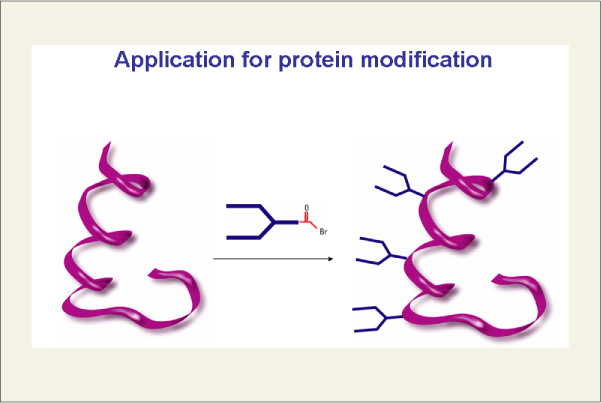
fig5






