研究成果 -Reserch-
糖ペプチドの合成
糖鎖ペプチドは、ペプチドの固相合成を利用して合成するのが一般的です。この場合、ペプチド鎖を固相合成により調製しておき、最後に糖鎖とペプチドと結合させるConvergent法と糖鎖アミノ酸をペプチドの固相合成を行う際に併用して糖鎖ペプチドを合成するstepwise 法があります。N型糖鎖ペプチドの合成は、N型糖鎖を化学的に大量に調製することが困難なため、その合成例は、O結合型のものに比べ少ないのですが、最近では、N型のコア5糖の糖鎖が結合した、癌細胞の転移に関与する糖タンパク質エンプリンの大型フラグメントの合成に成功した例が中原、北條グループによって報告されています(Tetrahedron Lett. 2003, 44, 2961-2964)。しかし、シアル酸を有する複合型糖鎖を持つペプチドの固相合成は困難と考えられていました。それは、酸処理でシアリル結合(赤色の糖残基とその隣の糖残基の間の結合)が容易に加水分解されるため、固相合成の最終段階でペプチドを固相から切り出す酸処理でシアリル結合が容易に加水分解されることが問題だったからです。
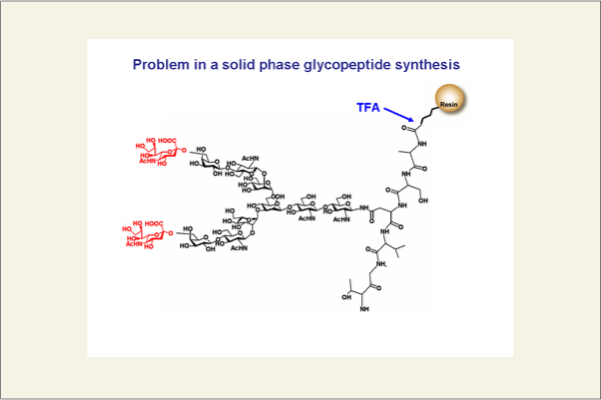
fig1
稲津グループは、 この点において有用な方法を報告しています(J. Am. Chem. Soc. 1999, 121, 284-290)。グルコサミン残基を1つだけ結合させたペプチドを固相合成により調製後、Endo-Mという酵素で複合型のシアリル糖鎖ブロックをそのグルコサミンに結合させ、天然型のシアリル糖鎖ペプチドを合成しています。我々は、それとは別に、鶏卵よりグラムスケールで得られる複合型のシアリル糖鎖を用いて糖鎖ペプチドの固相化学合成を検討することにしました。幸い、調製した複合型シアリル糖鎖のアスパラギン残基は既にFmoc 基で保護されているのでFmoc 法によるペプチド鎖が構築できます。しかし、シアル酸およびアスパラギンのカルボキシル基が遊離型なので、シアル酸のカルボキシル基を保護しておく必要がありました。
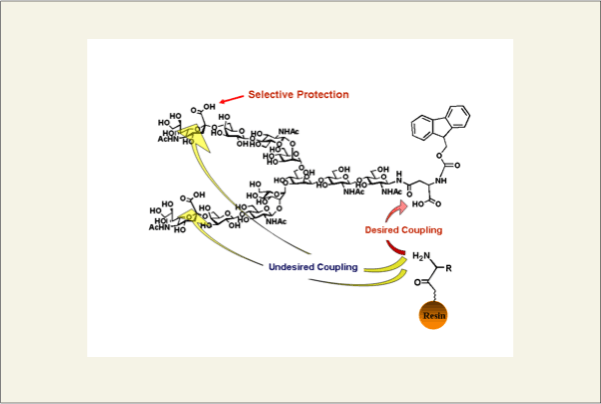
fig2
そこで、種々検討した結果、炭酸セシウム、ベンジルブロミドで処理すると選択的にシアル酸のカルボキシル基のみがエステル化されることを見い出しました。また、このエステル基がシアル酸に導入されることでペプチドを固相から切り出すために用いる95%トリフルオロ酢酸で長時間処理してもシアリル結合が加水分解されないことも見いだしました。
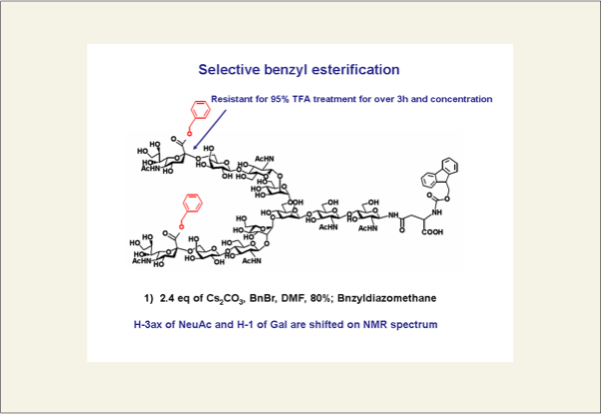
fig3
これにより卵黄より調製したシアリル糖鎖がペプチドの固相合成に十分利用できると考え、エリスロポエチンの78-83番をモデル配列としてシアリル糖鎖ペプチチドの合成を検討しました(Angew. Chem. Int. Ed. Engl. 2003, 42, 2537-2540)。まず、最初のFmocアミノ酸を固相の樹脂に結合させ、続いて、必要なアミノ酸を順次結合させ、そして、シアリル糖鎖アスパラギンをHATUにより縮合しました(収率38%)。そして、ペプチドをさらに伸長させるために、ペンタフルオロフェニル基で活性化したアミノ酸を順次反応させ目的とする配列を構築することができました。そして、95%トリフルオロ酢酸で3時間処理し、固相より目的とするシアリル糖鎖ペプチドを得ることができました。
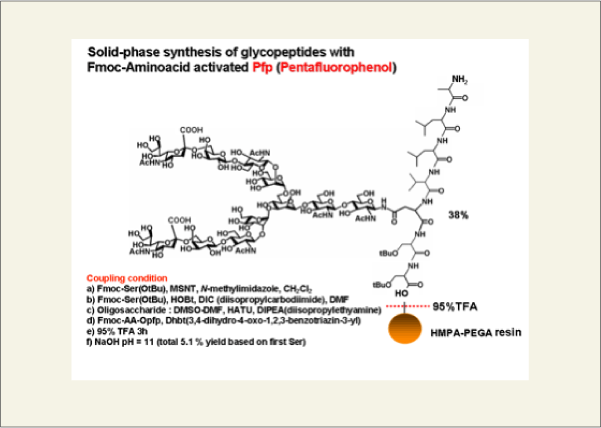
fig4
また、同様な方法を用いて、ペプチド鎖に違う構造の糖鎖を2本有するペプチドの合成にも応用することもできました(Chemistry Eur. J. 2004, 10, 971-985)。
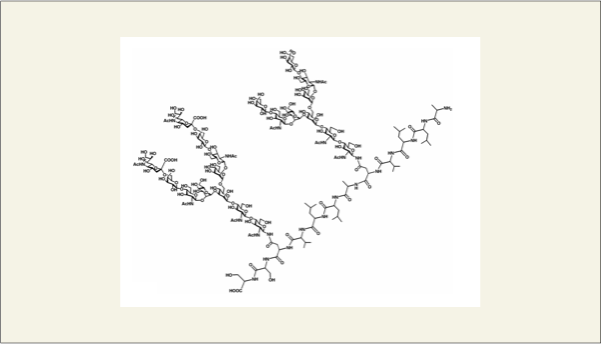
fig5






